Nguyên tắc điều chế kim loại là gì? Các phản ứng điều chế kim loại nào? Lập bản đồ tư duy và phương pháp sẵn sàng kim loại Làm sao? Bài tập điều chế kim loại cơ bản?… Trong phạm vi bài viết dưới đây, hãy cùng Cungdaythang.com tìm hiểu về chủ đề này nhé!
Nguyên tắc gia công kim loại
Thực hiện sự khử ion kim loại thành kim loại
(M ^ {n +} + ne mũi tên phải M)
Bình luận: Kim loại có tính khử mạnh khó điều chế hơn kim loại có tính khử yếu.
Các phương pháp điều chế kim loại
Phương pháp xử lý nhiệt
- Qui định:
Dùng chất khử như (C, CO, H_ {2},) hoặc kim loại hoạt động để loại trừ các ion kim loại ra khỏi hợp chất ở nhiệt độ cao.
Ví dụ: (PbO + H_ {2} overset {t ^ {circle}} {rightarrow} Pb + H_ {2} O)
(Fe_ {2} O_ {3} + 3CO overset {t ^ {circle}} {rightarrow} 2Fe + 3CO_ {2})
- Phạm vi vận dụng
Thường dùng để điều chế các kim loại có tính khử yếu (sau Al).
Phương pháp này được sử dụng rộng rãi trong công nghiệp.
Phương pháp luyện kim thủy lực
- Dùng chất khử mạnh Zn, Fe, .. để loại kim loại có tính khử yếu hơn trong dung dịch ra khỏi hợp chất.
(Fe + CuSO_ {4} overset {t ^ {circle}} {rightarrow} FeSO_ {4} + Cu)
(Fe + Cu ^ {2+} overset {t ^ {circle}} {rightarrow} Fe ^ {2+})
Chú ý:
- Cơ sở của phương pháp này là sử dụng các dung dịch thích hợp như (H_ {2} SO_ {4}, NaOH, NaCN, ..) để hoà tan kim loại hoặc hợp chất kim loại và tách nó ra khỏi phần ko tan. .
- Ko dùng kim loại kiềm, kiềm thổ để khử.
Phương pháp điện phân
Dùng dòng điện một chiều để khử các ion kim loại ở cực âm ra khỏi hợp chất.
- Cấu trúc của tế bào điện phân:
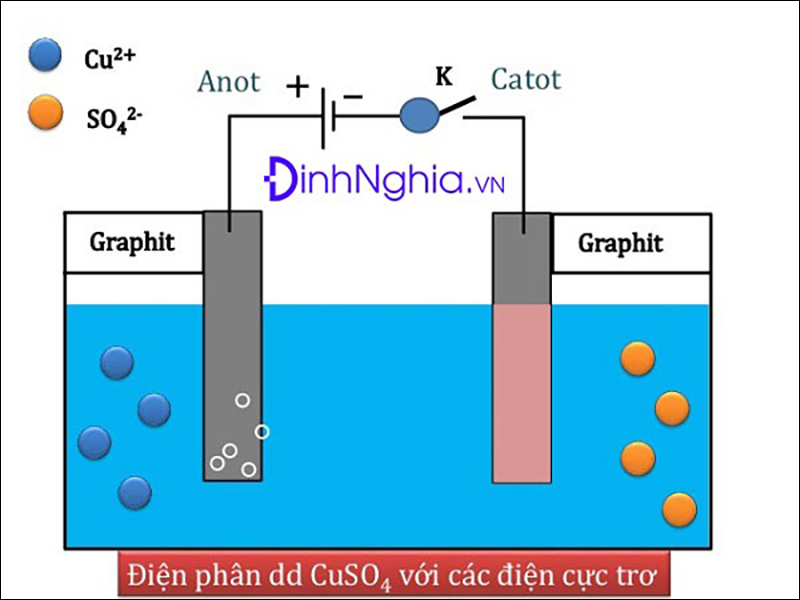
1 lọ hóa chất cần điện phân
Có 2 điện cực
- K (-) làm bằng graphit, graphit, Pt (điện cực trơ)
- A (+) làm bằng kim loại khác với Pt (điện cực ko trơ)
Nguồn điện một chiều: cực âm của nguồn điện nối với katot của bình điện phân, cực dương của nguồn điện nối với cực dương của bình điện phân.
- Cơ chế hoạt động của tế bào điện phân:
Dưới tác dụng của dòng điện một chiều, các ion chất điện li sẽ vận chuyển tới các điện cực
- Cation thành K (ion dương đối với cực âm)
- Anion thành A (ion âm cho cực dương)
Ở các điện cực xảy ra quá trình oxi hóa khử:
- Tại K: xảy ra quá trình oxi hóa
- Tại A: xảy ra quá trình khử.
- Điện phân hợp chất nóng chảy: Dùng để điều chế các kim loại mạnh như Na, K, Mg, Ca, …
Ví dụ: Điều chế NaCl nóng chảy thu được Na theo trật tự
(Bộ 2NaCl {dpnc} {rightarrow} 2Na + Cl_ {2})
- Điện phân dung dịch: Dùng để điều chế các kim loại yếu, trung bình bằng cách điện phân dung dịch muối của chúng.
Ví dụ: Điện phân dung dịch (CuCl_ {2}) thu được Cu về thứ p
(CuCl_ {2} bộ {dpdd} {rightarrow} Cu + Cl_ {2})
Tính khối lượng chất thu được ở mỗi điện cực. Dựa trên định luật Faraday:
(m = frac {AIt} {nF})
Trong đó:
- m: Khối lượng chất thu được trên mỗi điện cực (g)
- A: Khối lượng mol chất thu được ở điện cực
- n: Số electron nhưng mà nguyên tử hoặc ion đã cho hoặc nhận
- I: Dòng điện của ampe kế (A)
- t: Thời kì điện phân (giây)
- F: hằng số Faraday (F = 96500)
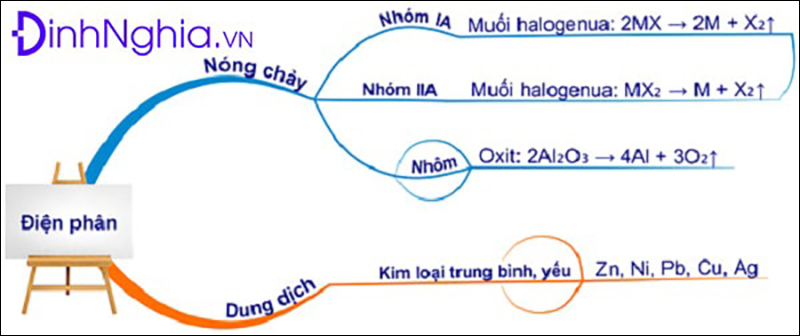
Một số dạng bài tập về gia công kim loại
Dạng 1: Dùng CO để khử (Fe_ {2} O_ {3})
- Nếu CO dư thì phản ứng xảy ra hoàn toàn.
(Fe_ {2} O_ {3} + CO mũi tên phải Fe + CO_ {2})
- Nếu phản ứng ko hoàn toàn: CO sẽ khử dần oxit sắt qua 3 thời đoạn:
(Fe_ {2} O_ {3} + CO mũi tên phải 2Fe_ {3} O_ {4} + CO_ {2})
(Fe_ {3} O_ {4} + CO mũi tên phải 3FeO + CO_ {2})
(FeO + CO mũi tên phải Fe + CO_ {2})
- Sử dụng công thức bảo toàn khối lượng:
(m_ {crg} = m_ {crbd} – m_ {crs} = m_ {Om})
(n_ {Om} = n_ {Opu} = n_ {CO_ {2} sr} = n_ {H_ {2} pu} = n_ {H_ {2} Osr})
Trong đó:
- (m_ {crg}) là khối lượng chất rắn đã giảm
- (m_ {crbd}) là khối lượng chất rắn ban sơ
- (m_ {crs}) là khối lượng của chất rắn sau phản ứng
- (m_ {Om}) là khối lượng của O bị mất
- (n_ {Om}) là số mol của O bị mất
- (n_ {Opu}) là số mol O đã phản ứng
- (n_ {CO_ {2} sr}) là số mol (CO_ {2}) được tạo ra
- (n_ {H_ {2} pu}) là số mol (H_ {2}) đã phản ứng
- (n_ {H_ {2} Osr}) là số mol (H_ {2} O) được tạo ra.

Dạng 2: Điều chế bằng phương pháp điện phân
Phương pháp:
- Khối lượng catot tăng là khối lượng kim loại tạo thành sau điện phân.
- (m_ {ddsdp} = m_ {ddtdp} – (m_ {kt} + m_ {k}))
Trong đó:
- (m_ {ddsdp}) là khối lượng dung dịch sau điện phân
- (m_ {ddtdp}) là khối lượng của dung dịch trước lúc điện phân
- (m_ {kt}) là khối lượng kết tủa
- (m_ {k}) là khối lượng của khí
Giảm thể tích dung dịch
(Delta m = m_ {kt} + m_ {k})
Lúc dung dịch bị điện phân,
- Tất cả các hiđroxit kim loại đều có phản ứng hóa học ((KOH, NaOH, Ba (OH) _ {2}, …))
- Axit oxy ((HNO_ {3}, H_ {2} SO_ {4}, HClO_ {4}, …))
- Muối được tạo thành bằng cách oxy hóa axit và bazơ kiềm ((KNO_ {3}, Na_ {2} SO_ {4}, …))
(mũi tên phải) Trên thực tiễn điện phân (H_ {2} O) để cho (H_ {2}) (ở cực âm) và (O_ {2}) (ở cực dương)
- Lúc điện phân một dung dịch với anot bằng kim loại ko trơ (ko dùng điện cực Pt hoặc than chì) thì ở anot chỉ xảy ra sự oxi hóa.
- Giữa mỗi cặp có thể xảy ra phản ứng phụ: chất tạo thành ở điện cực, chất tan trong dung dịch, chất dùng làm điện cực.
Supplydaythang.com đã phân phối cho bạn thông tin về phương pháp sẵn sàng kim loại, phản ứng điều chế kim loại, sơ đồ tư duy, phương pháp và bài tập điều chế kim loại cơ bản. Kỳ vọng những kiến thức trên sẽ hữu ích với bạn trong quá trình học tập của mình. Chúc may mắn với các nghiên cứu của bạn!
Phân mục: Câu hỏi thường gặp
# Phương pháp # điều chế # sản xuất # kim loại # và # hình thức # vật liệu chế tạo # có liên quan # vật liệu chế tạo
.u142c3d9f205e8b03d4ea4be9d1743e5c {padding: 0px; lề: 0; padding-top: 1em! important; padding-bottom: 1em! important; chiều rộng: 100%; hiển thị: khối; font-weight: bold; background-color: kế thừa; border: 0! important; border-left: 4px solid # 1ABC9C! important; box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -moz-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -o-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -webkit-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); văn bản-trang trí: ko có; } .u142c3d9f205e8b03d4ea4be9d1743e5c: active, .u142c3d9f205e8b03d4ea4be9d1743e5c: hover {opacity: 1; chuyển tiếp: độ mờ 250ms; webkit-chuyển đổi: độ mờ 250ms; văn bản-trang trí: ko có; } .u142c3d9f205e8b03d4ea4be9d1743e5c {chuyển tiếp: background-color 250ms; webkit-chuyển tiếp: background-color 250ms; độ mờ: 1; chuyển tiếp: độ mờ 250ms; webkit-chuyển đổi: độ mờ 250ms; } .u142c3d9f205e8b03d4ea4be9d1743e5c .ctaText {font-weight: bold; màu: # 16A085; văn bản-trang trí: ko có; font-size: 16px; } .u142c3d9f205e8b03d4ea4be9d1743e5c .postTitle {color: # 1ABC9C; text-decoration: gạch chân! quan trọng; font-size: 16px; } .u142c3d9f205e8b03d4ea4be9d1743e5c: hover .postTitle {text-decoration: underline! important; } Xem thêm: Công suất của bộ nguồn được xác định bởi
[toggle title=”xem thêm thông tin chi tiết về Phương pháp điều chế kim loại và các dạng bài tập liên quan” state=”close”]
Phương pháp điều chế kim loại và các dạng bài tập liên quan
Hình Ảnh về: Phương pháp điều chế kim loại và các dạng bài tập liên quan
Video về: Phương pháp điều chế kim loại và các dạng bài tập liên quan
Wiki về Phương pháp điều chế kim loại và các dạng bài tập liên quan
Phương pháp điều chế kim loại và các dạng bài tập liên quan -
Nguyên tắc điều chế kim loại là gì? Các phản ứng điều chế kim loại nào? Lập bản đồ tư duy và phương pháp sẵn sàng kim loại Làm sao? Bài tập điều chế kim loại cơ bản?… Trong phạm vi bài viết dưới đây, hãy cùng Cungdaythang.com tìm hiểu về chủ đề này nhé!
Nguyên tắc gia công kim loại
Thực hiện sự khử ion kim loại thành kim loại
(M ^ {n +} + ne mũi tên phải M)
Bình luận: Kim loại có tính khử mạnh khó điều chế hơn kim loại có tính khử yếu.
Các phương pháp điều chế kim loại
Phương pháp xử lý nhiệt
- Qui định:
Dùng chất khử như (C, CO, H_ {2},) hoặc kim loại hoạt động để loại trừ các ion kim loại ra khỏi hợp chất ở nhiệt độ cao.
Ví dụ: (PbO + H_ {2} overset {t ^ {circle}} {rightarrow} Pb + H_ {2} O)
(Fe_ {2} O_ {3} + 3CO overset {t ^ {circle}} {rightarrow} 2Fe + 3CO_ {2})
- Phạm vi vận dụng
Thường dùng để điều chế các kim loại có tính khử yếu (sau Al).
Phương pháp này được sử dụng rộng rãi trong công nghiệp.
Phương pháp luyện kim thủy lực
- Dùng chất khử mạnh Zn, Fe, .. để loại kim loại có tính khử yếu hơn trong dung dịch ra khỏi hợp chất.
(Fe + CuSO_ {4} overset {t ^ {circle}} {rightarrow} FeSO_ {4} + Cu)
(Fe + Cu ^ {2+} overset {t ^ {circle}} {rightarrow} Fe ^ {2+})
Chú ý:
- Cơ sở của phương pháp này là sử dụng các dung dịch thích hợp như (H_ {2} SO_ {4}, NaOH, NaCN, ..) để hoà tan kim loại hoặc hợp chất kim loại và tách nó ra khỏi phần ko tan. .
- Ko dùng kim loại kiềm, kiềm thổ để khử.
Phương pháp điện phân
Dùng dòng điện một chiều để khử các ion kim loại ở cực âm ra khỏi hợp chất.
- Cấu trúc của tế bào điện phân:

1 lọ hóa chất cần điện phân
Có 2 điện cực
- K (-) làm bằng graphit, graphit, Pt (điện cực trơ)
- A (+) làm bằng kim loại khác với Pt (điện cực ko trơ)
Nguồn điện một chiều: cực âm của nguồn điện nối với katot của bình điện phân, cực dương của nguồn điện nối với cực dương của bình điện phân.
- Cơ chế hoạt động của tế bào điện phân:
Dưới tác dụng của dòng điện một chiều, các ion chất điện li sẽ vận chuyển tới các điện cực
- Cation thành K (ion dương đối với cực âm)
- Anion thành A (ion âm cho cực dương)
Ở các điện cực xảy ra quá trình oxi hóa khử:
- Tại K: xảy ra quá trình oxi hóa
- Tại A: xảy ra quá trình khử.
- Điện phân hợp chất nóng chảy: Dùng để điều chế các kim loại mạnh như Na, K, Mg, Ca, ...
Ví dụ: Điều chế NaCl nóng chảy thu được Na theo trật tự
(Bộ 2NaCl {dpnc} {rightarrow} 2Na + Cl_ {2})
- Điện phân dung dịch: Dùng để điều chế các kim loại yếu, trung bình bằng cách điện phân dung dịch muối của chúng.
Ví dụ: Điện phân dung dịch (CuCl_ {2}) thu được Cu về thứ p
(CuCl_ {2} bộ {dpdd} {rightarrow} Cu + Cl_ {2})
Tính khối lượng chất thu được ở mỗi điện cực. Dựa trên định luật Faraday:
(m = frac {AIt} {nF})
Trong đó:
- m: Khối lượng chất thu được trên mỗi điện cực (g)
- A: Khối lượng mol chất thu được ở điện cực
- n: Số electron nhưng mà nguyên tử hoặc ion đã cho hoặc nhận
- I: Dòng điện của ampe kế (A)
- t: Thời kì điện phân (giây)
- F: hằng số Faraday (F = 96500)

Một số dạng bài tập về gia công kim loại
Dạng 1: Dùng CO để khử (Fe_ {2} O_ {3})
- Nếu CO dư thì phản ứng xảy ra hoàn toàn.
(Fe_ {2} O_ {3} + CO mũi tên phải Fe + CO_ {2})
- Nếu phản ứng ko hoàn toàn: CO sẽ khử dần oxit sắt qua 3 thời đoạn:
(Fe_ {2} O_ {3} + CO mũi tên phải 2Fe_ {3} O_ {4} + CO_ {2})
(Fe_ {3} O_ {4} + CO mũi tên phải 3FeO + CO_ {2})
(FeO + CO mũi tên phải Fe + CO_ {2})
- Sử dụng công thức bảo toàn khối lượng:
(m_ {crg} = m_ {crbd} - m_ {crs} = m_ {Om})
(n_ {Om} = n_ {Opu} = n_ {CO_ {2} sr} = n_ {H_ {2} pu} = n_ {H_ {2} Osr})
Trong đó:
- (m_ {crg}) là khối lượng chất rắn đã giảm
- (m_ {crbd}) là khối lượng chất rắn ban sơ
- (m_ {crs}) là khối lượng của chất rắn sau phản ứng
- (m_ {Om}) là khối lượng của O bị mất
- (n_ {Om}) là số mol của O bị mất
- (n_ {Opu}) là số mol O đã phản ứng
- (n_ {CO_ {2} sr}) là số mol (CO_ {2}) được tạo ra
- (n_ {H_ {2} pu}) là số mol (H_ {2}) đã phản ứng
- (n_ {H_ {2} Osr}) là số mol (H_ {2} O) được tạo ra.

Dạng 2: Điều chế bằng phương pháp điện phân
Phương pháp:
- Khối lượng catot tăng là khối lượng kim loại tạo thành sau điện phân.
- (m_ {ddsdp} = m_ {ddtdp} - (m_ {kt} + m_ {k}))
Trong đó:
- (m_ {ddsdp}) là khối lượng dung dịch sau điện phân
- (m_ {ddtdp}) là khối lượng của dung dịch trước lúc điện phân
- (m_ {kt}) là khối lượng kết tủa
- (m_ {k}) là khối lượng của khí
Giảm thể tích dung dịch
(Delta m = m_ {kt} + m_ {k})
Lúc dung dịch bị điện phân,
- Tất cả các hiđroxit kim loại đều có phản ứng hóa học ((KOH, NaOH, Ba (OH) _ {2}, ...))
- Axit oxy ((HNO_ {3}, H_ {2} SO_ {4}, HClO_ {4}, ...))
- Muối được tạo thành bằng cách oxy hóa axit và bazơ kiềm ((KNO_ {3}, Na_ {2} SO_ {4}, ...))
(mũi tên phải) Trên thực tiễn điện phân (H_ {2} O) để cho (H_ {2}) (ở cực âm) và (O_ {2}) (ở cực dương)
- Lúc điện phân một dung dịch với anot bằng kim loại ko trơ (ko dùng điện cực Pt hoặc than chì) thì ở anot chỉ xảy ra sự oxi hóa.
- Giữa mỗi cặp có thể xảy ra phản ứng phụ: chất tạo thành ở điện cực, chất tan trong dung dịch, chất dùng làm điện cực.
Supplydaythang.com đã phân phối cho bạn thông tin về phương pháp sẵn sàng kim loại, phản ứng điều chế kim loại, sơ đồ tư duy, phương pháp và bài tập điều chế kim loại cơ bản. Kỳ vọng những kiến thức trên sẽ hữu ích với bạn trong quá trình học tập của mình. Chúc may mắn với các nghiên cứu của bạn!
Phân mục: Câu hỏi thường gặp
# Phương pháp # điều chế # sản xuất # kim loại # và # hình thức # vật liệu chế tạo # có liên quan # vật liệu chế tạo
.u142c3d9f205e8b03d4ea4be9d1743e5c {padding: 0px; lề: 0; padding-top: 1em! important; padding-bottom: 1em! important; chiều rộng: 100%; hiển thị: khối; font-weight: bold; background-color: kế thừa; border: 0! important; border-left: 4px solid # 1ABC9C! important; box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -moz-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -o-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -webkit-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); văn bản-trang trí: ko có; } .u142c3d9f205e8b03d4ea4be9d1743e5c: active, .u142c3d9f205e8b03d4ea4be9d1743e5c: hover {opacity: 1; chuyển tiếp: độ mờ 250ms; webkit-chuyển đổi: độ mờ 250ms; văn bản-trang trí: ko có; } .u142c3d9f205e8b03d4ea4be9d1743e5c {chuyển tiếp: background-color 250ms; webkit-chuyển tiếp: background-color 250ms; độ mờ: 1; chuyển tiếp: độ mờ 250ms; webkit-chuyển đổi: độ mờ 250ms; } .u142c3d9f205e8b03d4ea4be9d1743e5c .ctaText {font-weight: bold; màu: # 16A085; văn bản-trang trí: ko có; font-size: 16px; } .u142c3d9f205e8b03d4ea4be9d1743e5c .postTitle {color: # 1ABC9C; text-decoration: gạch chân! quan trọng; font-size: 16px; } .u142c3d9f205e8b03d4ea4be9d1743e5c: hover .postTitle {text-decoration: underline! important; } Xem thêm: Công suất của bộ nguồn được xác định bởi
[rule_{ruleNumber}]
[box type=”note” align=”” class=”” border-radius: 5px; -webkit-border-radius: 5px; border: 2px solid #1c4a97; padding: 10px 20px;”>
Bạn đang xem: Phương pháp điều chế kim loại và các bài tập liên quan Trong Cungdaythang.com
Nguyên tắc điều chế kim loại là gì? Các phản ứng điều chế kim loại nào? Lập bản đồ tư duy và phương pháp chuẩn bị kim loại Làm sao? Bài tập điều chế kim loại cơ bản?… Trong phạm vi bài viết dưới đây, hãy cùng Cungdaythang.com tìm hiểu về chủ đề này nhé!
Nguyên tắc gia công kim loại
Thực hiện sự khử ion kim loại thành kim loại
(M ^ {n +} + ne mũi tên phải M)
Bình luận: Kim loại có tính khử mạnh khó điều chế hơn kim loại có tính khử yếu.

Các phương pháp điều chế kim loại
Phương pháp xử lý nhiệt
- Qui định:
Dùng chất khử như (C, CO, H_ {2},) hoặc kim loại hoạt động để loại bỏ các ion kim loại ra khỏi hợp chất ở nhiệt độ cao.
Ví dụ: (PbO + H_ {2} overset {t ^ {circle}} {rightarrow} Pb + H_ {2} O)
(Fe_ {2} O_ {3} + 3CO overset {t ^ {circle}} {rightarrow} 2Fe + 3CO_ {2})
- Phạm vi áp dụng
Thường dùng để điều chế các kim loại có tính khử yếu (sau Al).
Phương pháp này được sử dụng rộng rãi trong công nghiệp.
Phương pháp luyện kim thủy lực
- Dùng chất khử mạnh Zn, Fe, .. để loại kim loại có tính khử yếu hơn trong dung dịch ra khỏi hợp chất.
(Fe + CuSO_ {4} overset {t ^ {circle}} {rightarrow} FeSO_ {4} + Cu)
(Fe + Cu ^ {2+} overset {t ^ {circle}} {rightarrow} Fe ^ {2+})
Chú ý:
- Cơ sở của phương pháp này là sử dụng các dung dịch thích hợp như (H_ {2} SO_ {4}, NaOH, NaCN, ..) để hoà tan kim loại hoặc hợp chất kim loại và tách nó ra khỏi phần không tan. .
- Không dùng kim loại kiềm, kiềm thổ để khử.
Phương pháp điện phân
Dùng dòng điện một chiều để khử các ion kim loại ở cực âm ra khỏi hợp chất.
- Cấu trúc của tế bào điện phân:

1 lọ hóa chất cần điện phân
Có 2 điện cực
- K (-) làm bằng graphit, graphit, Pt (điện cực trơ)
- A (+) làm bằng kim loại khác với Pt (điện cực không trơ)
Nguồn điện một chiều: cực âm của nguồn điện nối với katot của bình điện phân, cực dương của nguồn điện nối với cực dương của bình điện phân.
- Cơ chế hoạt động của tế bào điện phân:
Dưới tác dụng của dòng điện một chiều, các ion chất điện li sẽ di chuyển đến các điện cực
- Cation thành K (ion dương đối với cực âm)
- Anion thành A (ion âm cho cực dương)
Ở các điện cực xảy ra quá trình oxi hóa khử:
- Tại K: xảy ra quá trình oxi hóa
- Tại A: xảy ra quá trình khử.
- Điện phân hợp chất nóng chảy: Dùng để điều chế các kim loại mạnh như Na, K, Mg, Ca, …
Ví dụ: Điều chế NaCl nóng chảy thu được Na theo thứ tự
(Bộ 2NaCl {dpnc} {rightarrow} 2Na + Cl_ {2})
- Điện phân dung dịch: Dùng để điều chế các kim loại yếu, trung bình bằng cách điện phân dung dịch muối của chúng.
Ví dụ: Điện phân dung dịch (CuCl_ {2}) thu được Cu về thứ p
(CuCl_ {2} bộ {dpdd} {rightarrow} Cu + Cl_ {2})
Tính khối lượng chất thu được ở mỗi điện cực. Dựa trên định luật Faraday:
(m = frac {AIt} {nF})
Trong đó:
- m: Khối lượng chất thu được trên mỗi điện cực (g)
- A: Khối lượng mol chất thu được ở điện cực
- n: Số electron mà nguyên tử hoặc ion đã cho hoặc nhận
- I: Dòng điện của ampe kế (A)
- t: Thời gian điện phân (giây)
- F: hằng số Faraday (F = 96500)

Một số dạng bài tập về gia công kim loại
Dạng 1: Dùng CO để khử (Fe_ {2} O_ {3})
- Nếu CO dư thì phản ứng xảy ra hoàn toàn.
(Fe_ {2} O_ {3} + CO mũi tên phải Fe + CO_ {2})
- Nếu phản ứng không hoàn toàn: CO sẽ khử dần oxit sắt qua 3 giai đoạn:
(Fe_ {2} O_ {3} + CO mũi tên phải 2Fe_ {3} O_ {4} + CO_ {2})
(Fe_ {3} O_ {4} + CO mũi tên phải 3FeO + CO_ {2})
(FeO + CO mũi tên phải Fe + CO_ {2})
- Sử dụng công thức bảo toàn khối lượng:
(m_ {crg} = m_ {crbd} – m_ {crs} = m_ {Om})
(n_ {Om} = n_ {Opu} = n_ {CO_ {2} sr} = n_ {H_ {2} pu} = n_ {H_ {2} Osr})
Trong đó:
- (m_ {crg}) là khối lượng chất rắn đã giảm
- (m_ {crbd}) là khối lượng chất rắn ban đầu
- (m_ {crs}) là khối lượng của chất rắn sau phản ứng
- (m_ {Om}) là khối lượng của O bị mất
- (n_ {Om}) là số mol của O bị mất
- (n_ {Opu}) là số mol O đã phản ứng
- (n_ {CO_ {2} sr}) là số mol (CO_ {2}) được tạo ra
- (n_ {H_ {2} pu}) là số mol (H_ {2}) đã phản ứng
- (n_ {H_ {2} Osr}) là số mol (H_ {2} O) được tạo ra.

Dạng 2: Điều chế bằng phương pháp điện phân
Phương pháp:
- Khối lượng catot tăng là khối lượng kim loại tạo thành sau điện phân.
- (m_ {ddsdp} = m_ {ddtdp} – (m_ {kt} + m_ {k}))
Trong đó:
- (m_ {ddsdp}) là khối lượng dung dịch sau điện phân
- (m_ {ddtdp}) là khối lượng của dung dịch trước khi điện phân
- (m_ {kt}) là khối lượng kết tủa
- (m_ {k}) là khối lượng của khí
Giảm thể tích dung dịch
(Delta m = m_ {kt} + m_ {k})
Khi dung dịch bị điện phân,
- Tất cả các hiđroxit kim loại đều có phản ứng hóa học ((KOH, NaOH, Ba (OH) _ {2}, …))
- Axit oxy ((HNO_ {3}, H_ {2} SO_ {4}, HClO_ {4}, …))
- Muối được tạo thành bằng cách oxy hóa axit và bazơ kiềm ((KNO_ {3}, Na_ {2} SO_ {4}, …))
(mũi tên phải) Trên thực tế điện phân (H_ {2} O) để cho (H_ {2}) (ở cực âm) và (O_ {2}) (ở cực dương)
- Khi điện phân một dung dịch với anot bằng kim loại không trơ (không dùng điện cực Pt hoặc than chì) thì ở anot chỉ xảy ra sự oxi hóa.
- Giữa mỗi cặp có thể xảy ra phản ứng phụ: chất tạo thành ở điện cực, chất tan trong dung dịch, chất dùng làm điện cực.
Supplydaythang.com đã cung cấp cho bạn thông tin về phương pháp chuẩn bị kim loại, phản ứng điều chế kim loại, sơ đồ tư duy, phương pháp và bài tập điều chế kim loại cơ bản. Hy vọng những kiến thức trên sẽ hữu ích với bạn trong quá trình học tập của mình. Chúc may mắn với các nghiên cứu của bạn!
Chuyên mục: Câu hỏi thường gặp
# Phương pháp # điều chế # sản xuất # kim loại # và # hình thức # vật liệu chế tạo # có liên quan # vật liệu chế tạo
.u142c3d9f205e8b03d4ea4be9d1743e5c {padding: 0px; lề: 0; padding-top: 1em! important; padding-bottom: 1em! important; chiều rộng: 100%; hiển thị: khối; font-weight: bold; background-color: kế thừa; border: 0! important; border-left: 4px solid # 1ABC9C! important; box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -moz-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -o-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); -webkit-box-shadow: 0 1px 2px rgba (0, 0, 0, 0.17); văn bản-trang trí: không có; } .u142c3d9f205e8b03d4ea4be9d1743e5c: active, .u142c3d9f205e8b03d4ea4be9d1743e5c: hover {opacity: 1; chuyển tiếp: độ mờ 250ms; webkit-chuyển đổi: độ mờ 250ms; văn bản-trang trí: không có; } .u142c3d9f205e8b03d4ea4be9d1743e5c {chuyển tiếp: background-color 250ms; webkit-chuyển tiếp: background-color 250ms; độ mờ: 1; chuyển tiếp: độ mờ 250ms; webkit-chuyển đổi: độ mờ 250ms; } .u142c3d9f205e8b03d4ea4be9d1743e5c .ctaText {font-weight: bold; màu: # 16A085; văn bản-trang trí: không có; font-size: 16px; } .u142c3d9f205e8b03d4ea4be9d1743e5c .postTitle {color: # 1ABC9C; text-decoration: gạch chân! quan trọng; font-size: 16px; } .u142c3d9f205e8b03d4ea4be9d1743e5c: hover .postTitle {text-decoration: underline! important; } Xem thêm: Công suất của bộ nguồn được xác định bởi [/box]
#Phương #pháp #điều #chế #kim #loại #và #các #dạng #bài #tập #liên #quan
[/toggle]
Bạn thấy bài viết Phương pháp điều chế kim loại và các dạng bài tập liên quan có khắc phục đươc vấn đề bạn tìm hiểu ko?, nếu ko hãy comment góp ý thêm về Phương pháp điều chế kim loại và các dạng bài tập liên quan bên dưới để thpttranhungdao.edu.vn có thể thay đổi & cải thiện nội dung tốt hơn cho độc giả nhé! Cám ơn bạn đã ghé thăm Website Trường THPT Trần Hưng Đạo
Phân mục: Là gì?
#Phương #pháp #điều #chế #kim #loại #và #các #dạng #bài #tập #liên #quan


Trả lời