Bảng tuần hoàn hóa học cứng cáp quen thuộc với bất kỳ bạn học trò nào. Từ thời cấp 2 tới lúc lên cấp 3, chúng ta xem hóa trị, các chỉ số đều nhờ nó. Tuy nhiên một số người vẫn chưa hiểu hết được thông tin trong bảng tuần hoàn các nguyên tố hoá học. Để phục vụ tốt nhất việc học hoá các lớp 8, 9, 10, 11, 12, NgonAZ đã làm một Bảng Tuần Hoàn Hoá Học Trực tuyến có sẵn liên kết trực tiếp với tất cả nguyên tố (giúp hiểu sâu hơn từng nguyên tố), thêm nữa có cả bảng tính tan, dãy điện hoá của kim loại và dãy hoạt động của kim loại rất dễ xem, dễ tìm hiểu sâu về các nguyên tố hoá học nhất có thể.
(Bảng tuần hoàn các nguyên tố hoá học này các bạn nên xem trên máy tính để hiện đầy đủ nhất thông tin)
Lịch sử ra đời của bảng tuần hoàn hóa học
Từ thời xa xưa, chúng ta đã biết tới nhiều nguyên tố hóa học như đồng, vàng, bạc, chì, sắt, thủy ngân,… Tới năm 1869, đã có khoảng 63 nguyên tố được tìm ra.
Vào năm 1862, J. Dobereiner đã có phát hiện quan trọng lúc thấy khối lượng nguyên tử của Stronti ở giữa khối lượng nguyên tử của hai nguyên tố Bari và Canxi. Bộ ba nguyên tố này có tính chất tương tự nhau. Sau đó, các nhà khoa học tiếp tục tìm thấy các bộ ba khác với quy luật như trên.
Tới năm 1862, người trước tiên nghĩ tới việc sắp xếp các nguyên tố hóa học theo chiều tăng của khối lượng nguyên tử lên 1 băng giấy là nhà địa chất Pháp De Chancourtois. Ông thấy tính chất của các nguyên tố giống tính chất của các con số. Tính chất đó lặp lại sau mỗi 7 nguyên tố.
Năm 1864, nhà hóa học người Anh John Newlands tìm ra được quy luật, mỗi nguyên tố hóa học đều trình bày tính chất tương tự như nguyên tố thứ 8 lúc xếp các nguyên tố theo khối lượng nguyên tử tăng dần.
Đặc thù một dấu ấn quan trọng khác cho ra đời bảng tuần hoàn hóa học, vào năm 1860, nhà bác học người Nga Mendeleev đã lên ý tưởng xây dựng bảng tuần hoàn các nguyên tố hóa học. Sau đó 9 năm, năm 1869, bảng “Bảng tuần hoàn các nguyên tố hóa học” trước tiên.
Tới năm 1870, nhà khoa học người Đức Lothar Mayer cũng nghiên cứu và cho ra đời bảng tuần hoàn hóa học tương tự như Mendeleev.

Bảng tuần hoàn hóa học có bao nhiêu nguyên tố?
Nếu đang thắc mắc bảng tuần hoàn hóa học có tất cả bao nhiêu nguyên tố thì theo thống kê mới nhất gồm 118 nguyên tố. Tính từ lúc nguyên tố 1 (Hidro) tới 118 (Oganesson).
Với việc xác nhận nguyên tố 113 là nguyên tố hóa học, Liên Minh Quốc Tế về Hóa Học cơ bản và ứng dụng IUPAC chính thức đưa 3 nguyên tố khác tuần tự 115, 117 và 118. Sự cập nhật này cho thấy chu kỳ 7 đã được lấp đầy. Bảng tuần hoàn cũng hoàn thiện hơn giống như khả năng tiên tri cách đây 200 năm của Mendeleev. Tri thức của nhân loại đã có thêm nhiều bước tiến quan trọng.
Điểm đặc trưng của 4 nguyên tố là 113, 115, 117 và 117 là khả năng tồn tại trong tự nhiên rất thấp, chỉ chưa tới 1 giây trước lúc vỡ ra thành nguyên tố khác. Chúng thuộc nguyên tố nặng nhất trong bảng tuần hoàn và chưa từng được thấy tồn tại bên ngoài phòng thí nghiệm.
Kết luận:
– Trong 118 nguyên tố hóa học, có tới 98 nguyên tố xuất hiện trong tự nhiên, 20 nguyên tố còn lại từ Ensteini tới Oganesson, chỉ xuất hiện trong phép tổng hợp nhân tạo.
– Trong 98 nguyên tố tự nhiên, có 84 nguyên tố xuất hiện nguyên thủy lúc Trái Đất tạo nên. Còn 14 nguyên tố chỉ xuất hiện trong chuỗi phân rã của các nguyên tố trên. Ko có nguyên tố nào nặng hơn Einsteini (số hiệu 99) từng quan sát thấy với lượng vĩ mô ở dạng tinh khiết.

Cấu tạo của bảng tuần hoàn hóa học
Cấu tạo của bảng tuần hoàn hóa học được phân thành 3 phần chính.
Phần thứ nhất: Ô nguyên tố
Nếu nhìn vào ô nguyên tố, bạn sẽ biết các thông tin như sau:
- Tên nguyên tố
- Ký hiệu hóa học
- Số hiệu nguyên tử
- Nguyên tử khối của nguyên tố đó
Số hiệu nguyên tử có số trị bằng số đơn vị điện tích hạt nhân và bằng số electron trong nguyên tử. Đây cũng là số trật tự của nguyên tố trong bảng tuần hoàn.
Ví dụ: Số hiệu nguyên tử của Photpho là 15 cho thấy:
- Photpho ở ô số 15
- Điện tích hạt nhân nguyên tử Photpho là 15+ (hay số đơn vị điện tích hạt nhân là 15)
- Có 15 electron trong nguyên tử Photpho
Phần thứ hai: Chu kỳ
Chu kỳ được khái niệm là dãy các nguyên tố nhưng mà nguyên tử của chúng có cùng số lớp electron và được xếp theo chiều điện tích hạt nhân tăng dần.
Bảng tuần hoàn gồm 7 chu kỳ. Trong đó chu kỳ nhỏ là 1, 2, 3. Còn chu kỳ lớn là 4, 5, 6, 7.
- Chu kỳ 1: Có 2 nguyên tố H và He, gồm 1 lớp electron trong nguyên tử. Điện tích hạt nhân tăng từ H là 1+ tới He là 2+.
- Chu kỳ 2: Có 8 nguyên tố từ Li tới Ne, gồm 2 lớp electron trong nguyên tử. Điện tích hạt nhân tăng từ Li là 3+, … tới Ne là 10+.
- Chu kỳ 3: Có 8 nguyên tố từ Na tới Ar, gồm 3 lớp electron trong nguyên tử. Điện tích hạt nhân tăng dần từ Na 11+, … tới Ar 18+.
- Chu kỳ 4 và chu kỳ 5: Mỗi chu kỳ đều có 18 nguyên tố, khởi đầu là một kim loại kiềm K 19+ và Rb 37+. Kết thúc là một khí trơ Kr 36+ và Xe là 54+.
- Chu kỳ 6: Có 32 nguyên tố, diễn ra từ kim loại kiềm Cs 55+ và kết thúc là khí trơ Rn 86+.
- Chu kỳ 7: Vẫn chưa hoàn thành.
Phần thứ ba: Nhóm nguyên tố
Nhóm nguyên tố là nhiều nguyên tố có số electron lớp ngoài cùng bằng nhau. Do đó tính chất tương tự nhau được xếp thành cột theo chiều tăng của điện tích hạt nhân nguyên tử. Số trật tự của nhóm bằng số electron lớp ngoài cùng của nguyên tử.
Có 2 loại nhóm nguyên tố là nhón A và nhóm B:
– Nhóm A: Gồm các nguyên tố s và p. Số thứ nhóm A = tổng số electron lớp ngoài cùng.
– Nhóm B: Gồm các nguyên tố d và f có cấu hình electron nguyên tử thì tận cùng ở dạng (n-1)dxnsy:
- Nếu (x+y) = 3 -> 7 thì nguyên tố thuộc nhóm (x+y)B.
- Nếu (x+y) = 8 -> 10 thì nguyên tố thuộc nhóm VIIIB.
- Nếu (x+y) > 10 thì nguyên tố thuộc nhóm (x+y-10)B
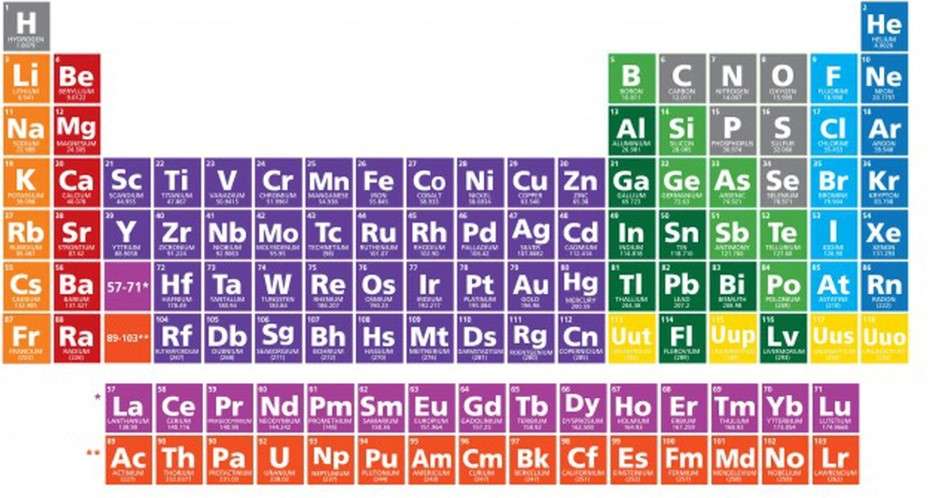
Cách xem bảng tuần hoàn hóa học
Để đọc được bảng tuần hoàn hóa học ko hề khó chút nào. Bạn có thể tự mình đọc thuần thục các nguyên tố nhờ thông tin dưới đây.
– Tên nguyên tố: Gồm một kiểu nguyên tử, được phân biệt bởi số hiệu nguyên tử, là số lượng proton có trong mỗi hạt nhân.
– Ký hiệu hóa học: Cũng là tên viết tắt của một nguyên tố. Biểu tượng của chúng gồm 1 hoặc 2 chữ cái trong bảng chữ cái Latin, được biết bởi chữ cái trước tiên viết in hoa.
– Số nguyên tử: Là số proton của nguyên tố hóa học được tìm thấy trong hạt nhân của 1 nguyên tử. Số nguyên tử giúp xác định duy nhất một nguyên tố hóa học. Số nguyên tử cũng bằng số electron trong một nguyên tử trung hòa về điện.
– Số oxi hóa: Là số áp cho một nguyên tử hay nhóm nguyên tử. Nhờ số oxi hóa, bạn biết được số electron trao đổi lúc một chất bị oxi hóa hoặc bị khử trong một phản ứng.
– Nguyên tử khối trung bình: Có nhiều đồng vị là nguyên tử khối trung bình của hỗn hợp các đồng vị có tính tới tỉ lệ phần trăm số nguyên tử tương ứng.
– Độ âm điện: Là khả năng hút electron của nguyên tử đó lúc tạo thành liên kết hóa học. Bạn cần nhớ, độ âm điện của nguyên tử nguyên tố càng lớn thì tính phi kim nguyên tố đó càng mạnh và trái lại.
– Cấu hình electron: Cho biết sự phân bố các electron trong lớp vỏ nguyên tử ở các trạng thái năng lượng không giống nhau hay ở các vùng hiện diện của chúng.
Cách học thuộc bảng tuần hoàn hóa học
Bảng tuần hoàn hóa học có tới 118 nguyên tố không giống nhau. Việc học thuộc hết tương đối khó. Tuy nhiên bạn vẫn cần nắm bắt những nguyên tố chính thường gặp. Chúng tôi sẽ méc bạn vài cách học thuộc bảng tuần hoàn hóa học nhanh nhất nhé.
Học thuộc bảng tuần hoàn qua cách truyền thống
– Nhận mặt các thành phần mỗi nguyên tố: Bạn nên ghi nhớ số nguyên tử, nguyên tử khối, độ âm điện, tên nguyên tố, ký hiệu hóa học,… của những nguyên tố quan trọng.
– Học vài nguyên tố mỗi ngày: Bạn có thể học chậm nhưng mà chắc bằng cách ghi nhớ vài nguyên tố mỗi ngày. Nhớ ôn tập lại nguyên tố cũ, tránh trường hợp học cái mới lại quên cái cũ.
– Dán bảng tuần hoàn khắp nơi: Nếu ko có nhiều thời kì thì việc dán bảng tuần hoàn cũng rất hiệu quả. Bạn thấy chúng ở mọi nơi trong nhà thì ghi nhớ sẽ dễ dàng hơn.
– Làm thẻ ghi chú cho mỗi nguyên tố: Thẻ ghi chú hay flashcard được nhận định giúp nhớ tri thức lâu hơn. Bạn mang chúng đi khắp nơi vừa tiện lại còn dễ ghi nhớ.
– Phân chia thời kì & cách học hợp lý: Mỗi người đều có quỹ thời kì không giống nhau. Việc học sẽ hiệu quả nếu bạn chủ động tìm hiểu. Hãy tận dụng mọi thời kì như giờ ra chơi, đi xe buýt,… rèn luyện tri thức của mình nhé.

Học thuộc bảng tuần hoàn bằng mẹo nhỏ
Mã hóa các chữ cái thành câu nói
- Nhóm IA: Hai, Li, Nào, Ko, Rót, Cà, Fe (H, Li, Na, K, Rb, Cs, Fr)
- Nhóm IIA: Banh, Mồm, Cá, Sấu, Bẻ, Răng (Be, Mg, Ca, Sr, Ba, Ra)
- Nhóm IIA: Bố, Người nào, Gáy, Inh, Tai (B, Al, Ga, In, Tl)
- Nhóm IV: Chú, Sỉ, Gọi em, Sang nhắm, Phở bò (C, Si, Ge, Sn, Pb)
- Nhóm V: Nhà, Phương, Ăn, Sống, Bí (N, P, As, Sb, Bi)
- Nhóm VI: Ông, Say, Sỉn, Té, Pò (O, S, Se, Te, Po)
- Nhóm VII: Phải, Chi, Nhỏ, Yêu, Anh (F, Cl, Br, I, At)
- Nhóm VIII: Hằng, Nga, Ăn, Khúc, Xương, Rồng (He, Ne, Ar, Kr, Xe, Rn)
Nhớ câu nói thân thuộc
Vững chắc bạn quen thuộc với câu nói: “Lúc nào cần may áo giáp sắt nhớ sang phố hỏi shop Á Phi Âu”. Trong câu nói này có 16 nguyên tố hóa học quan trọng gồm, F, Na, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au.
Hay câu nói: “Lâu nay ko rảnh coi phim” để chỉ 6 nguyên tố nhóm IA: Li, Na, K, Rb, Cs, Pr.
Bài ca hóa trị
Nếu thích vần vè một tí, bạn có thể học thuộc dễ dàng bảng tuần hoàn hóa học nhờ bài ca hóa trị I và bài ca hóa trị II.
| Bài ca hóa trị I | Bài ca hóa trị II |
| Kali (K), iốt (I), hidrô (H) Natri (Na) với bạc (Ag), clo (Cl) một loài Là hoá trị (I) hỡi người nào Nhớ ghi cho kỹ khỏi hoài phân vân Magiê (Mg), kẽm (Zn) với thuỷ ngân (Hg) Ôxi (O), đồng(Cu), thiếc (Sn) thêm phần bari (Ba) Cuối cùng thêm chữ canxi (Ca) Hoá trị II nhớ có gì khó khăn! Này nhôm (Al) hoá trị III lần In sâu sự ghi nhớ lúc cần có ngay Cácbon (C), silic (Si) này đây Có hoá trị IV ko ngày nào quên Sắt (Fe) kia lắm lúc hay phiền II, III rồi sẽ nhớ liền nhau thôi Lại gặp nitơ (N) khổ rồi I, II, III, IV lúc thời lên V Lưu huỳnh (S) lắm lúc chơi khăm Xuống II lên VI lúc nằm thứ IV Phốt pho (P) nói tới ko dư Có người nào hỏi tới, thì ừ rằng V Em ơi phấn đấu học chăm Bài ca hoá trị suốt năm cần dùng
| Hidro (H) cùng với liti (Li) Natri (Na) cùng với kali (K) chẳng rời Ngoài ra còn bạc (Ag) sáng ngời Chỉ mang hoá trị I thôi chớ nhầm Riêng đồng (Cu) cùng với thuỷ ngân (Hg) Thường II ít I chớ phân vân gì Thay đổi II, IV là chì (Pb) Tiêu biểu hoá trị của chì là II Bao giờ cũng hoá trị II Là ôxi (O), kẽm(Zn) chẳng sai chút gì Ngoài ra còn có canxi (Ca) Magiê (Mg) cùng với bari (Ba) một nhà Bo (B), nhôm (Al) thì hóa trị III Cácbon (C) silic (Si) thiếc (Sn) là IV thôi Thế nhưng phải nói thêm lời Hóa trị II vẫn là nơi đi về Sắt (Fe) II suy tính bộn bề Ko bền nên dễ biến liền sắt III Phốtpho III ít gặp nhưng mà Photpho V chính người ta gặp nhiều Nitơ (N) hoá trị bao nhiêu? I, II, III, IV phần nhiều tới V Lưu huynh lắm lúc chơi khăm Lúc II lúc IV, VI tăng tột cùng Clo (Cl), Iot (I) lung tung II III V VII thường thì I thôi Mangan rối rắm nhất đời Đổi từ I tới VII thời mới yên Hoá trị II dùng rất nhiều Hoá trị VII cũng được yêu hay cần Bài ca hoá trị thuộc lòng Viết thông công thức phòng ngừa quên lãng Học hành phấn đấu cần chuyên Siêng ôn chăm luyện tất nhiên nhớ nhiều |
Chơi các trò trực tuyến
Ngoài giờ học, bạn cũng có thể rèn luyện sự ghi nhớ và tiêu khiển nhờ trò chơi trực tuyến. Điều này được nhận định vô cùng hữu ích. Một số trang web có ứng dụng trò chơi như: Scratch, Elemental Flash Cards Quiz,…

Câu hỏi thường gặp về bảng tuần hoàn
Rất nhiều câu hỏi liên quan tới bảng tuần hoàn các nguyên tố hoá học nhưng mà mình thấy nhiều bạn hỏi:
Số hiệu nguyên tử là gì?
Số hiệu nguyên tử của một nguyên tố bằng tổng số hạt proton trong hạt nhân của các nguyên tử của nguyên tố đó. Số nguyên tử có thể cung ứng cái nhìn thâm thúy về cấu hình điện tử của nguyên tố. Ví dụ, cacbon có cấu hình electron là [He] 2s 2 2p 2 , vì số hiệu nguyên tử của nó là 6.
Số hiệu nguyên tử và số khối là gì?
Số proton và số nơtron sẽ xác định số khối của một nguyên tố. Vì các đồng vị của một nguyên tố có số khối hơi không giống nhau, nên nó tính khối lượng nguyên tử bằng cách lấy số khối lượng trung bình của các đồng vị của nó.
Hai nguyên tố không giống nhau có thể có cùng số hiệu nguyên tử được ko?
Các nguyên tử từ hai nguyên tố không giống nhau có thể có cùng số nơtron, nhưng ko bao giờ có cùng số proton. Số proton là duy nhất của nguyên tố và nó đại diện cho số nguyên tử.
Làm thế nào để chúng tôi tính toán khối lượng nguyên tử?
Thêm khối lượng của proton và nơtron để tính khối lượng nguyên tử của một nguyên tử của một nguyên tố. Ví dụ: Tìm khối lượng nguyên tử của đồng vị cacbon có 7 nơtron. Từ bảng tuần hoàn, bạn có thể thấy rằng cacbon có số nguyên tử là 6, là số proton của nó.
Vì sao số nguyên tử lại quan trọng?
Số hiệu nguyên tử được gọi là số proton trong nguyên tử. Con số này rất quan trọng, vì nó là duy nhất cho các nguyên tử của một nguyên tố nhất mực. Nguyên tử của một nguyên tố đều có cùng số proton và mỗi nguyên tố có số proton không giống nhau trong nguyên tử của nó.
Kết luận
Tương tự là bạn đã biết các thông tin quan trọng về bảng tuần hoàn hóa học. Ngoài ra, chúng tôi cũng méc bạn cách ghi nhớ nguyên tố nhanh chóng, xác thực nhất. Hi vọng thông tin trên sẽ giúp mọi người thích thú môn hóa hơn nhé.
Nhớ để nguồn bài viết này: Bảng Tuần Hoàn Hóa Học Online Mới Chuẩn Nhất 2022 của website thpttranhungdao.edu.vn
Phân mục: Kiến thức chung
#Bảng #Tuần #Hoàn #Hóa #Học #Trực tuyến #Mới #Chuẩn #Nhất


Trả lời