muối cacbonat được phân thành nhiều loại không giống nhau với những tính chất và ứng dụng cụ thể. Cùng Trường THPT Trần Hưng Đạo tìm hiểu kỹ hơn về loại muối này và giải các bài tập trong SGK qua bài viết dưới đây.
Nêu khái niệm muối cacbonat?
Muối cacbonat là muối của axit cacbonic, nó bao gồm hai loại phụ: muối cacbonat CO32- và hiđrocacbonat HCO3-. Muối cacbonat rất phổ quát và có nhiều ứng dụng trong đời sống như làm vật liệu sản xuất vôi, xi măng, xà phòng, thuốc chữa bệnh, v.v.
Phân loại muối cacbonat
Muối cacbonat được phân thành 2 loại chính gồm muối cacbonat trung tính và muối cacbonat axit.
Muối cacbonat trung hòa: Gọi là muối cacbonat do trong thành phần axit-bazơ ko còn nguyên tố H. Ví dụ: Magiê cacbonat (MgCO3), canxi cacbonat (CaCO3), natri cacbonat (Na2CO3)…
Muối cacbonat axit: Chúng được gọi là muối hiđrocacbonat, tức là chúng có nguyên tố H trong gốc axit. Ví dụ: Natri bicacbonat NaHCO3; canxi bicacbonat (Ca(HCO3)2, kali bicacbonat (KHCO3)…
Độ tan của muối cacbonat
Hồ hết các muối cacbonat đều ko tan trong nước, trừ một số muối cacbonat của kim loại kiềm như Na2CO3, K2CO3… Trái lại, hồ hết các muối hiđrocacbonat đều tan trong nước như Mg(HCO3)2, Ca(HCO3)2…
Tính chất hoá học của muối cacbonat
Muối cacbonat có những tính chất hóa học đặc trưng như phản ứng với dung dịch axit mạnh, phản ứng với dung dịch bazơ, phản ứng với dung dịch muối, dễ bị nhiệt phân hủy giải phóng khí CO2 (trừ Na2CO3, K2CO3…). Đặc trưng:

Muối cacbonat phản ứng với axit
Muối cacbonat có khả năng phản ứng với axit mạnh hơn axit cacbonic tạo thành muối mới và giải phóng khí CO2.
Để chứng minh tính chất hóa học này của muối cacbonat, SGK Hóa học 9 đã nêu các thí nghiệm cụ thể tuần tự cho dung dịch NaHCO3 và Na2CO3 phản ứng với dung dịch axit clohiđric (HCl). Quan sát thí nghiệm ta thấy ở cả 2 ống thử đều có hiện tượng bọt khí thoát ra. Điều này xảy ra do một phản ứng hóa học:
NaHCO3 (dd) + HCl (dd) -> NaCl (dd) + H2O (l) + CO2 (k)
Na2CO3 (dd) + 2HCl (dd) -> 2NaCl (dd) + H2O(l) + CO2 (k)
Phản ứng với dung dịch bazơ
Một số dung dịch muối cacbonat phản ứng với dung dịch bazơ tạo thành muối cacbonat ko tan và bazơ mới
Ví dụ:
K2CO3 (dd) + Ca(OH)2 (dd) -> CaCO3 (rắn – trắng) + 2KOH (dd)
Xem xét: Muối hiđrocacbonat phản ứng với dung dịch kiềm tạo thành muối trung hòa và nước.
Ví dụ:
NaHCO3 (đ) + NaOH (đ) -> Na2CO3 (đ) + H2O (l)
Phản ứng với dung dịch muối
Dung dịch muối cacbonat có thể phản ứng với một số dung dịch muối khác tạo ra 2 muối mới.
Ví dụ: Làm thí nghiệm cho dung dịch natri cacbonat (Na2CO3) phản ứng với dung dịch canxi clorua (CaCl2), xuất hiện kết tủa đục hoặc trắng. Ta có phương trình phản ứng sau:
Na2CO3 (dd) + CaCl2 (dd) -> CaCO3 (rắn – trắng) + 2NaCl (dd)
Phản ứng phân hủy muối cacbonat
Nhiều muối cacbonat, trừ muối cacbonat trung hòa của kim loại kiềm, dễ bị nhiệt phân hủy, giải phóng khí cacbonic. Ví dụ:
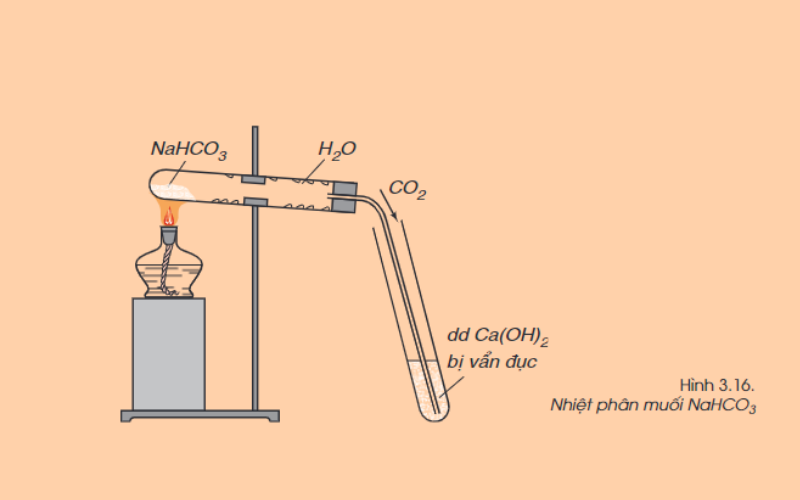
CaCO3(r) -> nhiệt độ CaO(r) + CO2(k)
2NaHCO3 (r) -> nhiệt độ Na2CO3 (r) + H2O (h) + CO2 (k)
Xem thêm:
- muối là gì? Tổng hợp kiến thức từ A-Z và bài tập thực hành
- Muối kali nitrat (KNO3): Khái niệm, tính chất, điều chế và ứng dụng
- Cacbon oxit (CO) là gì? Tính chất và ứng dụng phổ quát
Ứng dụng của muối cacbonat trong đời sống và sản xuất
Muối cacbonat có nhiều ứng dụng trong đời sống thực tiễn cũng như trong sản xuất công nghiệp. Mỗi loại muối cacbonat cụ thể đều có những ứng dụng riêng:

tên muối | Đăng kí |
CaCO3 (canxi cacbonat) | Ứng dụng trong ngành xây dựng như hoa cương, đá xây dựng, thành phần xi măng. Ứng dụng trong ngành sơn, canxi cacbonat được dùng làm chất độn chính. Ứng dụng làm tấm trần, khung nhựa, ống nhựa PVC… |
Na2CO3 (natri cacbonat) | Vật liệu sản xuất thủy tinh (chiếm 13-15%) Là một chất phụ gia trong xà phòng và chất tẩy rửa. Vật liệu cho nhiều thành phầm hóa học dựa trên natri. |
NaHCO3 (natri bicacbonat – muối nở) | Tạo độ giòn, xốp và thích mắt cho bánh. Tạo bọt và tăng pH trong một số loại thuốc như thuốc đau đầu. Khắc phục các vấn đề về răng mồm như ngăn ngừa sâu răng, mòn răng, nha chu… Ứng dụng bào chế các chế phẩm trung hòa acid dịch vị điều trị bệnh trào ngược dạ dày thực quản… |
Bài tập về muối cacbonat SGK Hóa học 9 có lời giải
Một số bài tập về muối cacbonat dành cho các bạn ôn tập kiến thức lý thuyết và vận dụng thực hành:

Bài tập 2 SGK Hóa học 9 trang 91
Dựa vào tính chất hóa học của muối cacbonat, hãy nêu tính chất của muối MgCO3 và viết các phương trình hóa học minh họa.
Câu trả lời gợi ý:
MgCO3 có tính chất của muối cacbonat.
Phản ứng với dung dịch axit:
MgCO3 + H2SO4 → MgSO4 + CO2↑ + H2O.
MgCO3 ko tan trong nước, ko phản ứng với dung dịch muối và dung dịch bazơ.
Dễ dàng phân hủy:
MgCO3 -> (nhiệt độ) MgO + CO2.
Bài tập 3 SGK Hóa học 9 trang 91
Viết các phương trình hóa học của các chuyển hóa sau:
C -> CO2 -> CaCO3 -> CO2
Câu trả lời gợi ý:
phương trình hóa học:
(1) C + O2 ->(nhiệt độ) CO2
(2) CO2 + Ca(OH)2 → CaCO3 + H2O
(3) CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Bài tập 4 SGK Hóa học 9 trang 91
Cho biết cặp chất nào sau đây có thể phản ứng với nhau.
a) H2SO4 và KHCO3; b) K2CO3 và NaCl; c) MgCO3 và HCl; d) CaCl2 và Na2CO3; e) Ba(OH)2 và K2CO3
Giảng giải và viết phương trình hóa học.
Câu trả lời gợi ý:
Những cặp chất phản ứng được với nhau là cặp chất a, c, d và e. Phương trình hóa học như sau:
H2SO4 + 2KHCO3 → K2SO4 + 2CO2 + 2H2O
MgCO3 + 2HCl → MgCl2 + CO2 + H2O
CaCl2 + Na2CO3 → CaCO3 + 2NaCl
Ba(OH)2 + K2CO3 → BaCO3 + 2KOH
Những cặp chất ko phản ứng với nhau: b).
Chú ý: Điều kiện xảy ra phản ứng trao đổi trong dung dịch chỉ lúc thành phầm tạo thành có kết tủa (ko tan) hoặc có khí tạo thành.
Bài tập 5 SGK Hóa học 9 trang 91
Tính thể tích khí CO2 (dktc) tạo thành để dập tắt đám cháy nếu trong bình chữa cháy có dung dịch chứa 980g H2SO4 tác dụng hết với dung dịch NaHCO3.
Câu trả lời gợi ý:
Phương trình hóa học của phản ứng:
2NaHCO3 + H2SO4 → Na2SO4 + 2CO2 + 2H2O
Tương tự: nCO2 = 2 x nH2SO4 = 10 x 2 = 20 mol.
VCO2 = nx 22,4 = 20 x 22,4 = 448 lít.
Trên đây là tổng quan toàn thể kiến thức lý thuyết về muối cacbonat và gợi ý cách giải một số bài tập trong SGK để độc giả tham khảo. Hãy thường xuyên ghé thăm website Trường THPT Trần Hưng Đạo để tham khảo thêm nhiều kiến thức môn học hay và đừng quên san sớt nếu thấy bài viết hữu ích nhé!
[toggle title=”xem thêm thông tin chi tiết về Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng” state=”close”]
Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng
Hình Ảnh về: Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng
Video về: Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng
Wiki về Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng
Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng -
muối cacbonat được phân thành nhiều loại không giống nhau với những tính chất và ứng dụng cụ thể. Cùng Trường THPT Trần Hưng Đạo tìm hiểu kỹ hơn về loại muối này và giải các bài tập trong SGK qua bài viết dưới đây.
Nêu khái niệm muối cacbonat?
Muối cacbonat là muối của axit cacbonic, nó bao gồm hai loại phụ: muối cacbonat CO32- và hiđrocacbonat HCO3-. Muối cacbonat rất phổ quát và có nhiều ứng dụng trong đời sống như làm vật liệu sản xuất vôi, xi măng, xà phòng, thuốc chữa bệnh, v.v.

Phân loại muối cacbonat
Muối cacbonat được phân thành 2 loại chính gồm muối cacbonat trung tính và muối cacbonat axit.
Muối cacbonat trung hòa: Gọi là muối cacbonat do trong thành phần axit-bazơ ko còn nguyên tố H. Ví dụ: Magiê cacbonat (MgCO3), canxi cacbonat (CaCO3), natri cacbonat (Na2CO3)…
Muối cacbonat axit: Chúng được gọi là muối hiđrocacbonat, tức là chúng có nguyên tố H trong gốc axit. Ví dụ: Natri bicacbonat NaHCO3; canxi bicacbonat (Ca(HCO3)2, kali bicacbonat (KHCO3)…
Độ tan của muối cacbonat
Hồ hết các muối cacbonat đều ko tan trong nước, trừ một số muối cacbonat của kim loại kiềm như Na2CO3, K2CO3… Trái lại, hồ hết các muối hiđrocacbonat đều tan trong nước như Mg(HCO3)2, Ca(HCO3)2…
Tính chất hoá học của muối cacbonat
Muối cacbonat có những tính chất hóa học đặc trưng như phản ứng với dung dịch axit mạnh, phản ứng với dung dịch bazơ, phản ứng với dung dịch muối, dễ bị nhiệt phân hủy giải phóng khí CO2 (trừ Na2CO3, K2CO3...). Đặc trưng:

Muối cacbonat phản ứng với axit
Muối cacbonat có khả năng phản ứng với axit mạnh hơn axit cacbonic tạo thành muối mới và giải phóng khí CO2.
Để chứng minh tính chất hóa học này của muối cacbonat, SGK Hóa học 9 đã nêu các thí nghiệm cụ thể tuần tự cho dung dịch NaHCO3 và Na2CO3 phản ứng với dung dịch axit clohiđric (HCl). Quan sát thí nghiệm ta thấy ở cả 2 ống thử đều có hiện tượng bọt khí thoát ra. Điều này xảy ra do một phản ứng hóa học:
NaHCO3 (dd) + HCl (dd) -> NaCl (dd) + H2O (l) + CO2 (k)
Na2CO3 (dd) + 2HCl (dd) -> 2NaCl (dd) + H2O(l) + CO2 (k)
Phản ứng với dung dịch bazơ
Một số dung dịch muối cacbonat phản ứng với dung dịch bazơ tạo thành muối cacbonat ko tan và bazơ mới
Ví dụ:
K2CO3 (dd) + Ca(OH)2 (dd) -> CaCO3 (rắn – trắng) + 2KOH (dd)
Xem xét: Muối hiđrocacbonat phản ứng với dung dịch kiềm tạo thành muối trung hòa và nước.
Ví dụ:
NaHCO3 (đ) + NaOH (đ) -> Na2CO3 (đ) + H2O (l)
Phản ứng với dung dịch muối
Dung dịch muối cacbonat có thể phản ứng với một số dung dịch muối khác tạo ra 2 muối mới.
Ví dụ: Làm thí nghiệm cho dung dịch natri cacbonat (Na2CO3) phản ứng với dung dịch canxi clorua (CaCl2), xuất hiện kết tủa đục hoặc trắng. Ta có phương trình phản ứng sau:
Na2CO3 (dd) + CaCl2 (dd) -> CaCO3 (rắn – trắng) + 2NaCl (dd)
Phản ứng phân hủy muối cacbonat
Nhiều muối cacbonat, trừ muối cacbonat trung hòa của kim loại kiềm, dễ bị nhiệt phân hủy, giải phóng khí cacbonic. Ví dụ:

CaCO3(r) -> nhiệt độ CaO(r) + CO2(k)
2NaHCO3 (r) -> nhiệt độ Na2CO3 (r) + H2O (h) + CO2 (k)
Xem thêm:
- muối là gì? Tổng hợp kiến thức từ A-Z và bài tập thực hành
- Muối kali nitrat (KNO3): Khái niệm, tính chất, điều chế và ứng dụng
- Cacbon oxit (CO) là gì? Tính chất và ứng dụng phổ quát
Ứng dụng của muối cacbonat trong đời sống và sản xuất
Muối cacbonat có nhiều ứng dụng trong đời sống thực tiễn cũng như trong sản xuất công nghiệp. Mỗi loại muối cacbonat cụ thể đều có những ứng dụng riêng:

tên muối | Đăng kí |
CaCO3 (canxi cacbonat) | Ứng dụng trong ngành xây dựng như hoa cương, đá xây dựng, thành phần xi măng. Ứng dụng trong ngành sơn, canxi cacbonat được dùng làm chất độn chính. Ứng dụng làm tấm trần, khung nhựa, ống nhựa PVC... |
Na2CO3 (natri cacbonat) | Vật liệu sản xuất thủy tinh (chiếm 13-15%) Là một chất phụ gia trong xà phòng và chất tẩy rửa. Vật liệu cho nhiều thành phầm hóa học dựa trên natri. |
NaHCO3 (natri bicacbonat - muối nở) | Tạo độ giòn, xốp và thích mắt cho bánh. Tạo bọt và tăng pH trong một số loại thuốc như thuốc đau đầu. Khắc phục các vấn đề về răng mồm như ngăn ngừa sâu răng, mòn răng, nha chu… Ứng dụng bào chế các chế phẩm trung hòa acid dịch vị điều trị bệnh trào ngược dạ dày thực quản... |
Bài tập về muối cacbonat SGK Hóa học 9 có lời giải
Một số bài tập về muối cacbonat dành cho các bạn ôn tập kiến thức lý thuyết và vận dụng thực hành:

Bài tập 2 SGK Hóa học 9 trang 91
Dựa vào tính chất hóa học của muối cacbonat, hãy nêu tính chất của muối MgCO3 và viết các phương trình hóa học minh họa.
Câu trả lời gợi ý:
MgCO3 có tính chất của muối cacbonat.
Phản ứng với dung dịch axit:
MgCO3 + H2SO4 → MgSO4 + CO2↑ + H2O.
MgCO3 ko tan trong nước, ko phản ứng với dung dịch muối và dung dịch bazơ.
Dễ dàng phân hủy:
MgCO3 -> (nhiệt độ) MgO + CO2.
Bài tập 3 SGK Hóa học 9 trang 91
Viết các phương trình hóa học của các chuyển hóa sau:
C -> CO2 -> CaCO3 -> CO2
Câu trả lời gợi ý:
phương trình hóa học:
(1) C + O2 ->(nhiệt độ) CO2
(2) CO2 + Ca(OH)2 → CaCO3 + H2O
(3) CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Bài tập 4 SGK Hóa học 9 trang 91
Cho biết cặp chất nào sau đây có thể phản ứng với nhau.
a) H2SO4 và KHCO3; b) K2CO3 và NaCl; c) MgCO3 và HCl; d) CaCl2 và Na2CO3; e) Ba(OH)2 và K2CO3
Giảng giải và viết phương trình hóa học.
Câu trả lời gợi ý:
Những cặp chất phản ứng được với nhau là cặp chất a, c, d và e. Phương trình hóa học như sau:
H2SO4 + 2KHCO3 → K2SO4 + 2CO2 + 2H2O
MgCO3 + 2HCl → MgCl2 + CO2 + H2O
CaCl2 + Na2CO3 → CaCO3 + 2NaCl
Ba(OH)2 + K2CO3 → BaCO3 + 2KOH
Những cặp chất ko phản ứng với nhau: b).
Chú ý: Điều kiện xảy ra phản ứng trao đổi trong dung dịch chỉ lúc thành phầm tạo thành có kết tủa (ko tan) hoặc có khí tạo thành.
Bài tập 5 SGK Hóa học 9 trang 91
Tính thể tích khí CO2 (dktc) tạo thành để dập tắt đám cháy nếu trong bình chữa cháy có dung dịch chứa 980g H2SO4 tác dụng hết với dung dịch NaHCO3.
Câu trả lời gợi ý:
Phương trình hóa học của phản ứng:
2NaHCO3 + H2SO4 → Na2SO4 + 2CO2 + 2H2O
Tương tự: nCO2 = 2 x nH2SO4 = 10 x 2 = 20 mol.
VCO2 = nx 22,4 = 20 x 22,4 = 448 lít.
Trên đây là tổng quan toàn thể kiến thức lý thuyết về muối cacbonat và gợi ý cách giải một số bài tập trong SGK để độc giả tham khảo. Hãy thường xuyên ghé thăm website Trường THPT Trần Hưng Đạo để tham khảo thêm nhiều kiến thức môn học hay và đừng quên san sớt nếu thấy bài viết hữu ích nhé!
[rule_{ruleNumber}]
[box type=”note” align=”” class=”” docs-internal-guid-29bd6966-7fff-b945-0c22-928d41899ad6″>
muối cacbonat được chia thành nhiều loại khác nhau với những tính chất và ứng dụng cụ thể. Cùng Trường THPT Trần Hưng Đạo tìm hiểu kỹ hơn về loại muối này và giải các bài tập trong SGK qua bài viết dưới đây.
Nêu khái niệm muối cacbonat?
Muối cacbonat là muối của axit cacbonic, nó bao gồm hai loại phụ: muối cacbonat CO32- và hiđrocacbonat HCO3-. Muối cacbonat rất phổ biến và có nhiều ứng dụng trong đời sống như làm nguyên liệu sản xuất vôi, xi măng, xà phòng, thuốc chữa bệnh, v.v.

Phân loại muối cacbonat
Muối cacbonat được phân thành 2 loại chính gồm muối cacbonat trung tính và muối cacbonat axit.
Muối cacbonat trung hòa: Gọi là muối cacbonat do trong thành phần axit-bazơ không còn nguyên tố H. Ví dụ: Magiê cacbonat (MgCO3), canxi cacbonat (CaCO3), natri cacbonat (Na2CO3)…
Muối cacbonat axit: Chúng được gọi là muối hiđrocacbonat, nghĩa là chúng có nguyên tố H trong gốc axit. Ví dụ: Natri bicacbonat NaHCO3; canxi bicacbonat (Ca(HCO3)2, kali bicacbonat (KHCO3)…
Độ tan của muối cacbonat
Hầu hết các muối cacbonat đều không tan trong nước, trừ một số muối cacbonat của kim loại kiềm như Na2CO3, K2CO3… Ngược lại, hầu hết các muối hiđrocacbonat đều tan trong nước như Mg(HCO3)2, Ca(HCO3)2…
Tính chất hoá học của muối cacbonat
Muối cacbonat có những tính chất hóa học đặc trưng như phản ứng với dung dịch axit mạnh, phản ứng với dung dịch bazơ, phản ứng với dung dịch muối, dễ bị nhiệt phân hủy giải phóng khí CO2 (trừ Na2CO3, K2CO3…). Đặc biệt:

Muối cacbonat phản ứng với axit
Muối cacbonat có khả năng phản ứng với axit mạnh hơn axit cacbonic tạo thành muối mới và giải phóng khí CO2.
Để chứng minh tính chất hóa học này của muối cacbonat, SGK Hóa học 9 đã nêu các thí nghiệm cụ thể lần lượt cho dung dịch NaHCO3 và Na2CO3 phản ứng với dung dịch axit clohiđric (HCl). Quan sát thí nghiệm ta thấy ở cả 2 ống nghiệm đều có hiện tượng bọt khí thoát ra. Điều này xảy ra do một phản ứng hóa học:
NaHCO3 (dd) + HCl (dd) -> NaCl (dd) + H2O (l) + CO2 (k)
Na2CO3 (dd) + 2HCl (dd) -> 2NaCl (dd) + H2O(l) + CO2 (k)
Phản ứng với dung dịch bazơ
Một số dung dịch muối cacbonat phản ứng với dung dịch bazơ tạo thành muối cacbonat không tan và bazơ mới
Ví dụ:
K2CO3 (dd) + Ca(OH)2 (dd) -> CaCO3 (rắn – trắng) + 2KOH (dd)
Lưu ý: Muối hiđrocacbonat phản ứng với dung dịch kiềm tạo thành muối trung hòa và nước.
Ví dụ:
NaHCO3 (đ) + NaOH (đ) -> Na2CO3 (đ) + H2O (l)
Phản ứng với dung dịch muối
Dung dịch muối cacbonat có thể phản ứng với một số dung dịch muối khác tạo ra 2 muối mới.
Ví dụ: Làm thí nghiệm cho dung dịch natri cacbonat (Na2CO3) phản ứng với dung dịch canxi clorua (CaCl2), xuất hiện kết tủa đục hoặc trắng. Ta có phương trình phản ứng sau:
Na2CO3 (dd) + CaCl2 (dd) -> CaCO3 (rắn – trắng) + 2NaCl (dd)
Phản ứng phân hủy muối cacbonat
Nhiều muối cacbonat, trừ muối cacbonat trung hòa của kim loại kiềm, dễ bị nhiệt phân hủy, giải phóng khí cacbonic. Ví dụ:

CaCO3(r) -> nhiệt độ CaO(r) + CO2(k)
2NaHCO3 (r) -> nhiệt độ Na2CO3 (r) + H2O (h) + CO2 (k)
Xem thêm:
- muối là gì? Tổng hợp kiến thức từ A-Z và bài tập thực hành
- Muối kali nitrat (KNO3): Định nghĩa, tính chất, điều chế và ứng dụng
- Cacbon oxit (CO) là gì? Thuộc tính và ứng dụng phổ biến
Ứng dụng của muối cacbonat trong đời sống và sản xuất
Muối cacbonat có nhiều ứng dụng trong đời sống thực tiễn cũng như trong sản xuất công nghiệp. Mỗi loại muối cacbonat cụ thể đều có những ứng dụng riêng:

tên muối | Đăng kí |
CaCO3 (canxi cacbonat) | Ứng dụng trong ngành xây dựng như đá hoa cương, đá xây dựng, thành phần xi măng. Ứng dụng trong ngành sơn, canxi cacbonat được dùng làm chất độn chính. Ứng dụng làm tấm trần, khung nhựa, ống nhựa PVC… |
Na2CO3 (natri cacbonat) | Nguyên liệu sản xuất thủy tinh (chiếm 13-15%) Là một chất phụ gia trong xà phòng và chất tẩy rửa. Nguyên liệu cho nhiều sản phẩm hóa học dựa trên natri. |
NaHCO3 (natri bicacbonat – muối nở) | Tạo độ giòn, xốp và đẹp mắt cho bánh. Tạo bọt và tăng pH trong một số loại thuốc như thuốc đau đầu. Giải quyết các vấn đề về răng miệng như ngăn ngừa sâu răng, mòn răng, nha chu… Ứng dụng bào chế các chế phẩm trung hòa acid dịch vị điều trị bệnh trào ngược dạ dày thực quản… |
Bài tập về muối cacbonat SGK Hóa học 9 có lời giải
Một số bài tập về muối cacbonat dành cho các bạn ôn tập kiến thức lý thuyết và vận dụng thực hành:

Bài tập 2 SGK Hóa học 9 trang 91
Dựa vào tính chất hóa học của muối cacbonat, hãy nêu tính chất của muối MgCO3 và viết các phương trình hóa học minh họa.
Câu trả lời gợi ý:
MgCO3 có tính chất của muối cacbonat.
Phản ứng với dung dịch axit:
MgCO3 + H2SO4 → MgSO4 + CO2↑ + H2O.
MgCO3 không tan trong nước, không phản ứng với dung dịch muối và dung dịch bazơ.
Dễ dàng phân hủy:
MgCO3 -> (nhiệt độ) MgO + CO2.
Bài tập 3 SGK Hóa học 9 trang 91
Viết các phương trình hóa học của các chuyển hóa sau:
C -> CO2 -> CaCO3 -> CO2
Câu trả lời gợi ý:
phương trình hóa học:
(1) C + O2 ->(nhiệt độ) CO2
(2) CO2 + Ca(OH)2 → CaCO3 + H2O
(3) CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Bài tập 4 SGK Hóa học 9 trang 91
Cho biết cặp chất nào sau đây có thể phản ứng với nhau.
a) H2SO4 và KHCO3; b) K2CO3 và NaCl; c) MgCO3 và HCl; d) CaCl2 và Na2CO3; e) Ba(OH)2 và K2CO3
Giải thích và viết phương trình hóa học.
Câu trả lời gợi ý:
Những cặp chất phản ứng được với nhau là cặp chất a, c, d và e. Phương trình hóa học như sau:
H2SO4 + 2KHCO3 → K2SO4 + 2CO2 + 2H2O
MgCO3 + 2HCl → MgCl2 + CO2 + H2O
CaCl2 + Na2CO3 → CaCO3 + 2NaCl
Ba(OH)2 + K2CO3 → BaCO3 + 2KOH
Những cặp chất không phản ứng với nhau: b).
Chú ý: Điều kiện xảy ra phản ứng trao đổi trong dung dịch chỉ khi sản phẩm tạo thành có kết tủa (không tan) hoặc có khí tạo thành.
Bài tập 5 SGK Hóa học 9 trang 91
Tính thể tích khí CO2 (dktc) tạo thành để dập tắt đám cháy nếu trong bình chữa cháy có dung dịch chứa 980g H2SO4 tác dụng hết với dung dịch NaHCO3.
Câu trả lời gợi ý:
Phương trình hóa học của phản ứng:
2NaHCO3 + H2SO4 → Na2SO4 + 2CO2 + 2H2O
Như vậy: nCO2 = 2 x nH2SO4 = 10 x 2 = 20 mol.
VCO2 = nx 22,4 = 20 x 22,4 = 448 lít.
Trên đây là tổng quan toàn bộ kiến thức lý thuyết về muối cacbonat và gợi ý cách giải một số bài tập trong SGK để bạn đọc tham khảo. Hãy thường xuyên ghé thăm website Trường THPT Trần Hưng Đạo để tham khảo thêm nhiều kiến thức môn học hay và đừng quên chia sẻ nếu thấy bài viết hữu ích nhé!
[/box]
#Muối #cacbonat #Khái #niệm #phân #loại #tính #chất #và #ứng #dụng
[/toggle]
Bạn thấy bài viết Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng có khắc phục đươc vấn đề bạn tìm hiểu ko?, nếu ko hãy comment góp ý thêm về Muối cacbonat: Khái niệm, phân loại, tính chất và ứng dụng bên dưới để thpttranhungdao.edu.vn có thể thay đổi & cải thiện nội dung tốt hơn cho độc giả nhé! Cám ơn bạn đã ghé thăm Website Trường THPT Trần Hưng Đạo
Phân mục: Giáo dục
#Muối #cacbonat #Khái #niệm #phân #loại #tính #chất #và #ứng #dụng

Trả lời